INTRODUCTION
Viren sind Krankheitserreger, die bei Transplantatempfängern besonders problematisch sind, da die Frage der Virusinfektionen bei Transplantationen ein komplexes Gleichgewicht zwischen den verschiedenen Virusinfektionen, die ein Patient im Laufe seines Lebens haben kann, der antiviralen Immunantwort des Empfängers und dem für die Gewährleistung eines funktionierenden Transplantats erforderlichen Grad der Immunsuppression widerspiegelt.
Die Infektion mit dem Polyomavirus BK (BKV) ist ein auftretendes Problem bei Nierentransplantationen und gilt als Preis für die moderne und starke Immunsuppression (IS).
BIOLOGISCHE ASPEKTE DES VIRUS
Das Polyomavirus gehört zusammen mit dem Papillomavirus zur Familie der Papoviren-Erreger. Das BK-Virus (BKV) gehört zusammen mit anderen beim Menschen nachgewiesenen Polyomaviren wie dem JC-Virus (JCV), dem KI-Virus, dem WU-Virus, dem Merkelzellkarzinom-Virus und dem Simian-Virus 40 (SV40) zur Familie der Polyomaviren.
Dabei handelt es sich um kleine, unbehüllte Viren mit einem Durchmesser von 42 nm. Das Kapsid hat eine ikosaedrische Symmetrie und beherbergt ein doppelzirkuläres Kettengenom aus DNA mit über 5000 Basenpaaren, das aus einer „frühen“ Region besteht, die hoch konserviert ist und für das „T/t-Antigen“ (TAg) kodiert, das an der Transformation, der viralen Replikation und der Genregulation und -expression beteiligt ist; und eine „späte“ Region, die für die drei Kapsidproteine, bekannt als VP1, VP2 und VP3, und für ein Protein namens „Agnoprotein“ kodiert, eine nicht-kodierende regulatorische Region, die zwischen den beiden anderen liegt und in der sich die Determinanten für die Replikation, die TAg-Verbindung und Elemente der Transkriptionsregulation befinden.
Das Polyomavirus besitzt eine Anpassungsspezifität an seinen Wirt; daher ist seine Evolution wahrscheinlich mit der Evolution der Wirtsspezies verbunden, so dass die natürliche Infektion nur bei einer begrenzten Anzahl eng verwandter Spezies vorkommt, was einen Marker für die Feststellung der Rassenunterschiede zwischen den Menschen darstellt.
Mit Hilfe von Gensequenzierungsanalysen wurden verschiedene Genotypen festgestellt: Europäer, Asiaten und Afrikaner. Der Rest der Genotypen entspricht Rekombinationen dieser drei, und obwohl sein Ursprung schwer zu bestimmen ist, könnte die Untersuchung dieses Virus ein Hilfsmittel für das Verständnis der Evolution menschlicher Migrationen sein.
BKV ist mit zwei Komplikationen verbunden, die bei Transplantatempfängern beobachtet werden: BK-Virus-assoziierte Nephropathie (BKVN) bei Nierentransplantationen und hämorrhagische Zystitis bei Knochenmarkstransplantationen. Im Gegensatz zum BKV ist das JCV zwar im Uroepithel beheimatet und wird normalerweise reaktiviert, verursacht aber selten eine Nephropathie, sondern ist mit multifokaler Leukoenzephalopathie und Enzephalitis assoziiert. SV40, das von Affen stammt, wurde durch mit Polio- und Adenoviren kontaminierte Impfstoffe in die menschliche Bevölkerung eingeschleppt, und obwohl sein Vorhandensein in transplantierten Nierenbiopsien nachgewiesen wurde, ist seine Bedeutung bei Nierentransplantationen noch nicht genau definiert.
EPIDEMIOLOGIE UND RISIKOFAKTOREN
Die Primärinfektion tritt subklinisch im ersten Lebensjahrzehnt auf, mit einer Seroprävalenz von über 80 % in der erwachsenen Bevölkerung.
Die Infektionsquelle ist ausschließlich der Mensch, es konnten keine Tiere als Reservoir nachgewiesen werden, und der Übertragungsweg kann fäkal-oral, respiratorisch, transplazentar und durch gespendetes Gewebe sein. Während der virämischen Phase infiziert das Virus die Gewebe, das Urothel, das Lymphgewebe und das Gehirn, wobei es zu einer latenten lytischen Infektion kommt.
Nach der natürlichen Virusübertragung im Säuglingsalter verbleibt das BKV in den Harnwegen mit intermittierenden Reaktivierungen und niedrigen Virurien (Vr), 5 %-10 % bei immunkompetenten Erwachsenen.1,2 Bei immungeschwächten Personen steigt die Häufigkeit von BK Vr auf 20-60 %, und noch höhere Werte von Virurie und das Auftreten von Decoy-Zellen im Urin sind ebenfalls häufig.3
Bei Nierentransplantierten oszilliert die Prävalenz von BK-Virus-assoziierten Nephropathien (BKVN) zwischen 1 % und 10 %,4 was eher auf die Immunsuppressionstherapie und die diagnostischen Methoden zurückzuführen ist als auf reale epidemiologische Unterschiede.
Im Jahr 2004 wurde die Behandlung der BKV-Infektion nach Nierentransplantation als Variable für die Entwicklung nach der Transplantation (TBKV) in die amerikanische Datenbank aufgenommen; die Daten wurden später analysiert und ergaben eine Gesamtzahl von >48 000 Transplantaten, von denen 1474 innerhalb von 24 Monaten behandelt wurden. Die kumulative Inzidenz der BKVN stieg mit der Zeit an, von 3,45 % nach 24 Monaten auf 6,6 % nach 60 Monaten nach der Transplantation.
Das Transplantatversagen als Folge der BKVN tritt in Zentren ohne Screening-Programme mit einer Rate von 50 % bis 100 % nach 24 Monaten auf, was die Bedeutung einer frühen Diagnose der Krankheit unterstreicht.5
Unterschiedliche IS-Protokolle wurden als Risikofaktoren für die Entwicklung von BKVN identifiziert, insbesondere die Verwendung von Dreifachtherapien mit antikineurinischen Medikamenten, Mycophenolatmofetil (MMF) und Steroiden,5,6 aber BKVN-Fälle wurden auch bei Verwendung anderer IS-Schemata beschrieben, was darauf hindeutet, dass die Intensität der IS-Behandlung und nicht das spezifische Medikament selbst der Risikofaktor in diesem Fall ist. Es gibt auch andere Arten von Risikofaktoren, wie z. B. Patientenfaktoren (Männer >50 Jahre alt, BKV-seronegativer Empfänger), Transplantatfaktoren (BKV-seropositiver Spender, HLA-Inkompatibilitäten, immunologische oder ischämische Verletzungen) und virale Faktoren (latente Viruslast, Kapsid-Serotyp und Replikationsfähigkeit).7
BKVN HISTOLOGISCHE DIAGNOSE UND VERLAUF
Dekozyten, Virurie und Virämie weisen nur auf eine virale Replikation hin, nicht auf eine Nephropathie, sind aber wichtige Hilfsmittel zur Prävention und Überwachung der Krankheit.
Das einzige klinische Zeichen der BKVN ist die Verschlechterung der Nierenfunktion, und wenn diese auftritt, ist es bereits zu spät, um einzugreifen, da die Nierenschädigung bereits eingetreten ist.
Die Diagnose der Erkrankung kann nur durch eine Transplantatbiopsie gestellt werden, bei der die typischen basophilen nukleären Viruseinschlüsse in den Epithelzellen (Tubulus, Bowman-Kapsel und/oder Urothel) und Entzündungszeichen mit Tubulitis (Abbildung 1A) gefunden werden, ähnliche Befunde, wie sie bei der akuten Transplantatabstoßung durch T-Zellen auftreten. Nur durch den Einsatz der immunhistochemischen Technik für SV-40 LTAg können wir eine positive Kernfärbung beobachten und das Polyomavirus (BK, JC) als das für die Entzündung verantwortliche identifizieren, wodurch die Diagnose der akuten T-Zell-Abstoßung verworfen (Abbildung 1B) und die Diagnose der BKVN bestätigt wird.
BKVN histologische Läsionen sind fokal und heterogen, so dass eine negative Biopsie die Diagnose nicht ausschließen kann. Daher muss dieser Test wiederholt werden, wenn die Viruslast im Blut des Patienten persistent hoch bleibt.
Die histologischen Muster der BKVN2,8,9 basieren auf der Identifizierung und Ausdehnung des entzündlichen Infiltrats und der Virusinfektions-assoziierten Fibrose, wodurch drei histologische Muster festgelegt werden können (Abbildung 2).
KLINISCHE EVOLUTION UND MÖGLICHKEITEN ZUR FRÜHZEITIGEN PRÄVENTION UND DIAGNOSE
Die allgemeine klinische Evolution der BKVN9 ist in Abbildung 3 dargestellt, die zeigt, wie die Entwicklung der Krankheit durch das Auftreten einer BK-Virurie (BK Vr) vorhergesagt wird, eine Folge der viralen Reaktivierung und Replikation im Harntrakt, mit dem Auftreten typischer Decoy-Zellen (Abbildung 4), die mit zytologischen Routinetests im Urin leicht zu identifizieren sind. Die Quantifizierung von Vr mittels PCR-Techniken ist jedoch empfindlicher als die Zytologie und ermöglicht die Unterscheidung zwischen BKV- und JCV-Infektionen.
Wenn die Virurie >105 Kopien/ml beträgt und persistiert, folgt Wochen oder Monate später die Entwicklung einer Virämie (Vm) bei >107 Kopien/ml und schließlich die BKVN. BK Vr ist nicht diagnostisch für eine Nierenparenchymschädigung, aber das gleichzeitige Auftreten von Vm und Vr ist pathognomonisch für eine Nierenparenchymschädigung (BKVN). Beibehaltene oder typischerweise steigende Vm ist ein prädiktiver Faktor für eine Verschlechterung der Nierenfunktion und korreliert mit dem Vorhandensein und der Schwere histologischer Läsionen. Bei Patienten mit normaler oder mäßig niedriger Nierenfunktion ist die Wahrscheinlichkeit, histologische Indikatoren für BKVN zu finden, direkt proportional zur Dauer und Schwere der Virämie. Erhöhte und anhaltende Virämie identifiziert jene Patienten mit unkontrollierter Virusreplikation, die zu einer Nierenschädigung führt.
Zusammenfassend lässt sich sagen, dass eine frühzeitige Diagnose und Intervention den Schaden für das Transplantat minimiert. Abbildung 5 zeigt einen Diagnosealgorithmus, der auf früheren Publikationen basiert.4,9
BKVN-BEHANDLUNG
Die beste Behandlung für BKVN ist eine frühe Diagnose der Krankheit, um zu handeln, bevor Nierenschäden entstehen.
Aus diesem Grund empfehlen die KDIGO-Leitlinien10 ein Screening-Verfahren für alle nierentransplantierten Patienten, indem die Vm-Werte während der ersten drei Monate (2D) und alle drei Monate bis zum Ende des ersten Jahres (2D) monatlich getestet werden, sowie immer dann, wenn eine Nierenfunktionsstörung ohne erkennbare alternative Ursache auftritt (2D), und nach der Behandlung einer Episode akuter Abstoßung (2D). Eine Reduktion der IS wird auch vorgeschlagen, wenn Vm dauerhaft größer als 107 Kopien/ml ist (2D).
Bezüglich der Reduktion der IS besteht der erste Schritt in der Umsetzung des Standardprotokolls (keine Gabe von CAN oder antiproliferativen Behandlungen oberhalb der für den therapeutischen Bereich angegebenen Werte), gefolgt von der Messung der Virämie alle 4 Wochen, der Reduktion von NAb um 15%-20%, der Reduktion von MMF und/oder MMF-Suppression um 50% und/oder dem Ersatz von TAC durch CsA oder ein ISP (Abbildung 6).11
Im Hinblick auf antivirale Behandlungen wurden i.v. Immunglobuline, Ciclofovir, Leflunomid und Chinolone empirisch eingesetzt, wobei ihre Wirksamkeit derzeit schwer zu bestimmen ist, da sie nicht in Kombination mit einer Reduktion der IS verabreicht wurden und weil kontrollierte und randomisierte prospektive Studien fehlen.
Abschließend möchten wir uns zur Nieren-Retransplantation bei Patienten äußern, die ein Transplantat aufgrund von BKVN verloren haben. Die Rezidivrate der Erkrankung liegt in Kurzstudien bei 12%. Die Empfehlungen, die in diesen Situationen beachtet werden müssen, sind: 1) den Patienten über das erhöhte potenzielle Risiko eines BKVN-Rezidivs zu informieren; 2) die Abwesenheit von Virusreplikation zu bestätigen (Blut- und Urin-PCR, wenn der Patient auf die Transplantationsliste aufgenommen wird und danach alle 6 Monate), der Patient muss das Transplantat mit negativen PCR-Ergebnissen aus Blutproben erhalten, und 3) den IS an die Pathologie anzupassen.12-14
KEY POINTS
1. Die starken und modernen Formen der Immunsuppression könnten für die zunehmende Prävalenz dieser Infektion verantwortlich sein
2. Eine BK-Virus-Infektion bei immunsupprimierten Patienten könnte die Funktion und das Überleben von Nierentransplantaten beeinträchtigen
3. Eine frühzeitige Diagnose durch strikte Überwachung der Urin-Dekozytenzahl und/oder Virurie und Virämie ist entscheidend, um die negativen Auswirkungen dieser Komplikation zu vermeiden
4. Es gibt keine Hinweise auf eine spezifische wirksame Behandlung dieser Infektion. Nur eine Reduzierung der Immunsuppression kann die Virulenz minimieren.
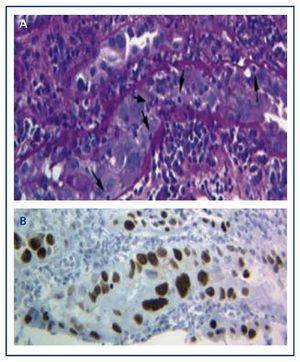
Abbildung 1. Basophile nukleäre Viruseinschlüsse in Epithelzellen und Tubulitis bei der BK-Virus-Nephropathie (a) und Immunhistochemie für das Antigen SV-40 LTAg (b)

Abbildung 2. Histologische Muster der BK-Virus-assoziierten Nephropathie
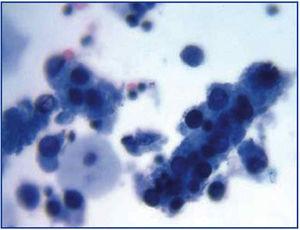
Abbildung 3. Disperse Decoy-Zellen und zelluläre Zylinder, die verdichtete Decoy-Zellen enthalten. Wenn sie erscheinen, sind diese Zylinder pathognomisch für Nierenschäden
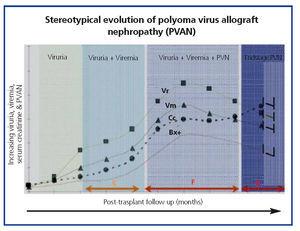
Abbildung 4. Phasen der Entwicklung der BK-Virus-assoziierten Nephropathie
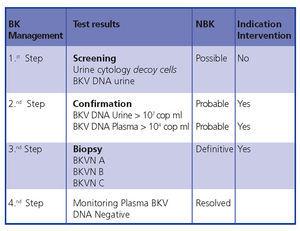
Abbildung 5. BKVN Diagnose-Algorithmus

Abbildung 6. BKVN-Behandlungsalgorithmus