Cyclophosphamid, auch Cytoxan genannt, wird als „zytotoxisches Mittel“ eingestuft, weil es auf viele Zelltypen („gute“ Zellen wie auch „schlechte“) toxisch wirkt. Cyclophosphamid gehört zu einer Reihe von Medikamenten, die zunächst als Chemotherapeutikum (ein Medikament zur Behandlung von Krebs) entwickelt wurden. Man entdeckte, dass Cyclophosphamid – zusätzlich zu seiner Nützlichkeit bei Krebs – auch eine bedeutende Fähigkeit hat, das Immunsystem zu unterdrücken. Daher ist das Medikament sehr wirksam bei der Behandlung von immunologisch vermittelten Krankheiten, einschließlich einiger Formen von Vaskulitis. Im Allgemeinen werden zur Behandlung von Vaskulitis viel niedrigere Dosen von Cyclophosphamid verwendet als zur Behandlung von Krebs. Dennoch sind die Dosen von Cyclophosphamid, die zur Behandlung von Vaskulitis eingesetzt werden, immer noch hoch genug, um eine beträchtliche Anzahl von Nebenwirkungen zu verursachen, und das Medikament muss mit großer Vorsicht eingesetzt werden.
In diesem Abschnitt werden die Nebenwirkungen von Cyclophosphamid besprochen. Nach dem Durchlesen der vielen möglichen Nebenwirkungen könnte ein vernünftiger Mensch zu dem Schluss kommen, dass die Behandlung schlimmer zu sein scheint als die Krankheit, die sie behandeln soll! Wir betonen jedoch, dass Cyclophosphamid bei einigen Formen der Vaskulitis, die auf Steroide (Prednison) allein nicht ansprechen, ein lebensrettendes Medikament sein kann. Zum Beispiel war vor der Einführung von Cyclophosphamid in der Behandlung der Wegener-Granulomatose in den 1970er Jahren die Wegener-Granulomatose fast ausnahmslos eine tödliche Krankheit, selbst mit hohen Dosen von Steroiden. Jetzt, mit der Kombination von Cyclophosphamid und Prednison, sprechen mehr als 90 % der Wegener-Patienten auf die Behandlung an, und 75 % erreichen eine Krankheitsremission. Andere Arten von Vaskulitis, bei denen Cyclophosphamid manchmal eingesetzt wird, sind: Polyarteriitis nodosa, mikroskopische Polyangiitis, das Churg-Strauss-Syndrom, Kryoglobulinämie, Vaskulitis des zentralen Nervensystems, rheumatoide Vaskulitis und andere Arten von Vaskulitis, die auf Prednison und andere Medikamente nicht ansprechen.
Cyclophosphamid wird normalerweise in Verbindung mit Steroiden (Prednison) eingesetzt. Es hilft häufig, die Dosen der Steroide zu verringern, die zur Kontrolle der Vaskulitis notwendig sind. In diesem Zusammenhang wird Cyclophosphamid manchmal auch als „steroidsparendes Mittel“ bezeichnet. Die möglichen Nebenwirkungen von Cyclophosphamid unterscheiden sich größtenteils von denen von Prednison. Zum Beispiel ist Cyclophosphamid im Gegensatz zu Prednison NICHT mit einer Gewichtszunahme, Knochenverdünnung, erhöhtem Blutdruck oder einer Tendenz zur Auslösung von Diabetes verbunden. Allerdings erhöht Cyclophosphamid das Risiko eines Patienten für bestimmte Arten von Infektionen (siehe unten) erheblich und hat mehrere andere potenziell sehr schwerwiegende Nebenwirkungen, einschließlich einer erhöhten Veranlagung für bestimmte Arten von Krebs. Wir besprechen die möglichen Nebenwirkungen von Cyclophosphamid im Folgenden.
Nebenwirkungen
Cyclophosphamid kann entweder intravenös (etwa einmal im Monat) oder oral (einmal am Tag, typischerweise in einer geringeren Dosis) verabreicht werden. Bis zu einem gewissen Grad unterscheiden sich die Nebenwirkungen von Cyclophosphamid je nach Art der Verabreichung des Medikaments.
- Infektion
- Knochenmarksuppression
- Krebs
- Blasenprobleme
- Unfruchtbarkeit
Infektion
Cyclophosphamid erhöht das Risiko für „opportunistische“ Infektionen, d.h. Infektionen, die das intakte Immunsystem einer Person normalerweise abwehren könnte. So erhöht Cyclophosphamid zwar nicht die Anfälligkeit eines Patienten für eine Erkältung, wohl aber das Risiko für schwerwiegendere Infektionen, darunter Tuberkulose, Pilzinfektionen und schwere Virusinfektionen. Einige spezifische Infektionen, die häufig mit der Einnahme von Cyclophosphamid (oder der Einnahme von Immunsuppressiva im Allgemeinen) verbunden sind, werden im Folgenden beschrieben:
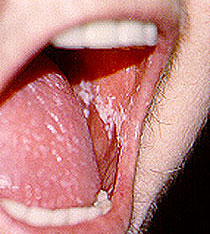
„Soor“ – Soor ist eine Pilzinfektion im Mund, die durch Candida verursacht wird. Sie zeigt sich in der Regel als weiße Flecken auf der Innenseite des Mundes (siehe Abbildung unten) und ist leicht mit der Verwendung von antimykotischen Mundspülungen oder -tropfen zu behandeln. Manchmal betreffen Candida-Infektionen auch die Speiseröhre (die „Nahrungsröhre“, die vom Mund zum Magen führt). Dieser Zustand, „Candida-Ösophagitis“ genannt, führt oft zu Schmerzen beim Schlucken und muss mit starken Anti-Pilz-Medikamenten wie Fluconazol behandelt werden.
„Gürtelrose“ – oder Herpes zoster. „Gürtelrose“ entsteht durch Reaktivierung des Virus, das Windpocken verursacht (Varicella zoster). Fast jeder, der heute älter als 5 Jahre ist, hatte schon einmal Windpocken, meist als Kind. Normalerweise bleibt das Virus, das die Krankheit verursacht hat, auch nach dem Abklingen des Ausschlags und der anderen Symptome der Windpocken in einem „schlafenden“ Zustand im Körper und versteckt sich in der Wurzel eines der Nerven entlang der Wirbelsäule. Jahrzehnte später, wenn das Immunsystem mit dem Alter etwas nachlässt (ein normaler Teil des Alterungsprozesses) oder wenn das Immunsystem unterdrückt wird (durch Medikamente wie Cyclophosphamid), wird das Virus wieder aktiv. Wenn es reaktiviert wird, verursacht Varizella Zoster in der Regel einen schmerzhaften Ausschlag in der Verteilung eines einzelnen Nervs, z. B. über eine Seite des Gesichts oder einen Arm hinunter. Der Ausschlag ist durch Gruppen von kleinen Bläschen (Blasen) gekennzeichnet, die auf einer Basis von geröteter Haut sitzen und extrem schmerzhaft sein können.
„Gürtelrose“ ist mit antiviralen Medikamenten wie Acyclovir oder Famcyclovir behandelbar. Diese sollten so schnell wie möglich eingeleitet werden. Auch narkotische Schmerzmittel können für mehrere Wochen notwendig sein. In einer kleinen Minderheit der Fälle führt die Gürtelrose zu Schmerzen, die über Monate anhalten können. Dieser Zustand wird „postherpetische Neuralgie“ genannt.
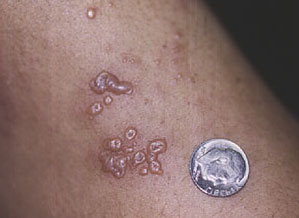
Ein Beispiel für den klassischen Ausschlag einer „Gürtelrose“.
Pneumocystis-carinii-Pneumonie („PCP“) – Pneumocystis carinii ist ein Pilz, der sich in der Lunge der meisten Menschen befindet. Menschen mit intaktem Immunsystem haben keine Probleme, den Organismus in Schach zu halten. Bei Patienten, die immunsupprimiert sind, kann der Organismus eine schwere Form der Lungenentzündung verursachen: PCP. Noch vor wenigen Jahren war PCP die häufigste Ursache für schwere Lungeninfektionen bei AIDS-Patienten. Aufgrund von Fortschritten bei der Behandlung und Vorbeugung dieser Erkrankung ist PCP heute ein viel selteneres Problem bei AIDS. In ähnlicher Weise kann PCP auch bei Patienten mit Vaskulitis verhindert werden, indem die Patienten bestimmte Arten von Antibiotika täglich oder jeden zweiten Tag einnehmen. Die für diesen Zweck am häufigsten verwendeten Antibiotika sind Trimethoprim-Sulfamethoxazol (Bactrim, Septra) oder, bei Patienten, die allergisch auf Sulfa-Medikamente reagieren, Dapson.
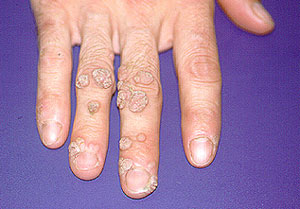
Warzen – Das Bild unten zeigt eine Vermehrung von Warzen bei einem Vaskulitis-Patienten unter Immunsuppression. Die Entwicklung von Warzen in diesem Ausmaß ist recht ungewöhnlich.
Knochenmarksuppression
Das Knochenmark ist das Organ des Körpers, das rote Blutkörperchen (die Sauerstoff transportieren), weiße Blutkörperchen (die Infektionen bekämpfen) und Blutplättchen (die bei der Blutgerinnung helfen) bildet. Bei fast allen Patienten, die mit Cyclophosphamid behandelt werden, kommt es zu einer gewissen Unterdrückung der Fähigkeit des Knochenmarks, diese lebenswichtigen Blutelemente zu produzieren. Daher ist eine sorgfältige Überwachung des Blutbildes während der Cyclophosphamid-Therapie unerlässlich. Die Unterdrückung des Knochenmarks durch Cyclophosphamid ist in der Regel vorübergehend – d. h. sie reagiert auf eine Verringerung der Dosis oder das Absetzen des Medikaments -, aber es können gefährlich niedrige Werte einer dieser drei Zelllinien (oder sogar ein dauerhaftes Versagen des Knochenmarks) auftreten.
Die weißen Blutkörperchen sind die Zelllinie, die in der Regel am empfindlichsten auf die Wirkung von Cyclophosphamid reagiert. Wenn Cyclophosphamid intravenös verabreicht wird, neigt die Anzahl der weißen Blutkörperchen dazu, ihren Tiefpunkt („Nadir“) zwischen 7 und 14 Tagen nach der Verabreichung zu erreichen. Daher sollten die Blutzellenwerte etwa 10 Tage nach der Verabreichung von Cyclophosphamid gemessen und so oft wie nötig wiederholt werden, um sicherzustellen, dass die Werte nicht zu niedrig werden. Dies bedeutet normalerweise, dass das Blutbild alle 2-4 Wochen kontrolliert wird. Wenn Cyclophosphamid oral verabreicht wird (d. h. täglich statt einmal im Monat), sollte das Blutbild etwa 7 Tage nach Beginn der Behandlung und dann nicht seltener als einmal alle 3 Wochen kontrolliert werden. In einigen Zentren, die Erfahrung in der Betreuung von Patienten mit Vaskulitis und der Anwendung von Cyclophosphamid haben, wird das Blutbild alle 2 Wochen kontrolliert.
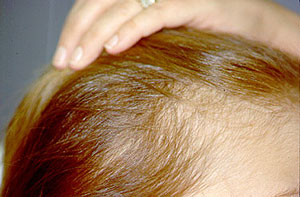
Abgebildet ist eine Frau mit mikroskopischer Polyangiitis, die mit intravenösem Cyclophosphamid und hohen Dosen von Kortikosteroiden behandelt wurde. Nach mehreren Cyclophosphamid-Behandlungen entwickelte sie eine deutliche (reversible) Ausdünnung ihrer Haare.
Krebs
Viele der Nebenwirkungen von Cyclophosphamid treten am ehesten auf, während der Patient das Medikament einnimmt. Bei diesen Nebenwirkungen sinkt das Risiko ihres Auftretens nach Absetzen des Medikaments stark ab. Im Gegensatz dazu kann das mit der Einnahme von Cyclophosphamid verbundene Krebsrisiko über viele Jahre bestehen bleiben, auch nachdem die Patienten das Medikament abgesetzt haben. Das Krebsrisiko scheint abhängig zu sein von der Dauer der Einnahme des Medikaments und der kumulativen Dosierung des Medikaments. Patienten, die Cyclophosphamid eingenommen haben, haben ein erhöhtes Risiko für mindestens zwei primäre Arten von Malignität: Leukämie/Lymphom und Blasenkrebs. Es kann auch ein erhöhtes Risiko für andere Krebsarten bestehen, aber die Risiken sind weniger hoch.
Leukämie/Lymphom – Eine der langfristigen Nebenwirkungen der Cyclophosphamid-Anwendung ist eine signifikante Erhöhung des Risikos von Knochenmark- und Lymphknotenkrebs (bekannt als Leukämie bzw. Lymphom). Ärzte können derzeit nicht vorhersagen, bei welchen Patienten ein Risiko für diese Komplikationen besteht. Das beste Mittel, um diese Krebsarten zu vermeiden, ist die umsichtige Anwendung von Cyclophosphamid: die niedrigstmögliche Dosis des Medikaments für die kürzeste Zeit, die notwendig ist, um die Krankheit zu kontrollieren.
Blasenkrebs – Cyclophosphamid hat die Tendenz, die Blase zu schädigen (siehe Blasenprobleme, unten). Diese Schädigung prädisponiert Patienten für die Entwicklung von Blasenkrebs. Das Risiko für Blasenkrebs (und für andere Blasenkomplikationen) ist größer, wenn Cyclophosphamid in der oralen Tagesform verabreicht wird. Bei Patienten mit Wegener-Granulomatose, die an den National Institutes of Health mit oralem täglichem Cyclophosphamid behandelt wurden, lag das Risiko für Blasenkrebs bei 6 %. Bei Patienten, die bis zu 15 Jahre lang nachbeobachtet wurden, lag die prognostizierte Inzidenz von Blasenkrebs sogar bei 16 %. Daher müssen Patienten, die mit Cyclophosphamid behandelt wurden, auf unbestimmte Zeit auf die Möglichkeit von Blasenkomplikationen der Behandlung überwacht werden. Die beste Methode zum Screening auf diese Komplikation ist die Überprüfung auf rote Blutkörperchen im Urin durch eine Urinanalyse, gefolgt von einer Zystoskopie, wenn rote Blutkörperchen vorhanden sind. Patienten, bei denen eine Blasenschädigung durch Cyclophosphamid, d. h. eine medikamenteninduzierte Zystitis, nachgewiesen wurde, sollten sich in regelmäßigen Abständen, die von ihren Urologen festgelegt werden, einer Überwachungszystoskopie unterziehen.
Wenn Cyclophosphamid intravenös verabreicht wird, kann gleichzeitig ein blasenschützendes Medikament namens MESNA gegeben werden. MESNA scheint den toxischen Metaboliten von Cyclophosphamid (Acrolein) zu neutralisieren, von dem angenommen wird, dass er für die Blasenkomplikationen verantwortlich ist. Zusätzliche Strategien zur Verringerung der Blasentoxizität von Cyclophosphamid umfassen: 1) intravenöse Flüssigkeitszufuhr vor der Einnahme von Cyclophosphamid; 2) Einnahme des gesamten Medikaments in einer einzigen morgendlichen Dosis und Herunterspülen mit einer großen Menge Flüssigkeit; und 3) Trinken von reichlich Flüssigkeit über den Tag verteilt (acht 8-Unzen-Gläser Wasser), um eine rege Urinausscheidung aufrechtzuerhalten.
Blasenprobleme
Zusätzlich zur Krebserkrankung kann Cyclophosphamid eine variable Menge von Blutungen aus der Blase verursachen, eine Komplikation, die als „hämorrhagische Zystitis“ bekannt ist. Diese Blutung kann von einigen wenigen roten Blutkörperchen im Urin (mit bloßem Auge nicht sichtbar; nur durch Untersuchung des Urins unter dem Mikroskop nachweisbar) bis hin zu lebensbedrohlichen Blutungen aus der Blase reichen. Wenn eine Blutung aus der Blase entdeckt wird, während ein Patient Cyclophosphamid einnimmt, sollte das Medikament abgesetzt werden, bis die Blase durch eine Blasenspiegelung untersucht werden kann.
Unfruchtbarkeit
Cyclophosphamid kann sowohl bei Männern als auch bei Frauen, die mit dem Medikament behandelt werden, Unfruchtbarkeit verursachen. Wie bei vielen Nebenwirkungen von Cyclophosphamid scheint das Risiko der Unfruchtbarkeit mit der Dauer der Behandlung (und wahrscheinlich auch mit der kumulativen Dosis) zusammenzuhängen. Auch das Alter einer Frau kann sich auf das Unfruchtbarkeitsrisiko auswirken, wobei das Auftreten einer frühen Menopause bei Frauen, die zum Zeitpunkt des Behandlungsbeginns über 30 Jahre alt sind, höher ist.
In einer Langzeitstudie zur Wirksamkeit von Cyclophosphamid bei der Behandlung von Lupus lag das Risiko für Unfruchtbarkeit bei Frauen im gebärfähigen Alter bei 57 %.