Objetivos
Después de completar esta sección, deberías ser capaz de
- escribir una ecuación para describir la formación de una cianohidrina a partir de un aldehído o una cetona.
- Identificar la cianohidrina formada a partir de la reacción de un aldehído o cetona dados con cianuro de hidrógeno.
- Identificar el aldehído o la cetona, los reactivos, o ambos, necesarios para preparar una cianohidrina dada.
- Escribir el mecanismo detallado para la adición de cianuro de hidrógeno a un aldehído o una cetona.
Asegúrese de que puede definir, y utilizar en su contexto, el término clave que aparece a continuación.
- cianohidrina
Notas de estudio
Para que la formación de la cianohidrina tenga éxito es importante tener iones de cianuro libres disponibles para reaccionar con la cetona o el aldehído. Esto se puede conseguir utilizando una sal (por ejemplo, KCN o NaCN) o una forma sililada (por ejemplo, Me3SiCN) de cianuro en condiciones ácidas o utilizando HCN con alguna base añadida para producir el nucleófilo CN- necesario.
El cianuro de hidrógeno (HC≡N), se añade de forma reversible a los aldehídos y a muchas cetonas formando aductos de hidroxialcanenitrilo (comúnmente conocidos y llamados como cianohidrinas). Las cianohidrinas tienen la fórmula estructural de R2C(OH)CN. La «R» de la fórmula representa un alquilo, un arilo o un hidrógeno.
Figura 19.6.1: Reacción general de formación de cianohidrina
Una característica importante de la formación de cianohidrina es que requiere un catalizador básico. Dado que el propio cianuro de hidrógeno es un ácido (pKa = 9,25), los mejores resultados se producen cuando una pequeña cantidad de una base fuerte activa el cianuro de hidrógeno convirtiéndolo en ion cianuro ((-)C≡N), que puede funcionar como nucleófilo del carbono. En ausencia de base, la reacción no se produce o, en el mejor de los casos, es muy lenta. La formación de la cianohidrina es débilmente exotérmica, y se ve favorecida por los aldehídos, y las cetonas cíclicas y metiladas sin obstáculos.
En las síntesis prácticas de cianohidrinas, es conveniente añadir un ácido fuerte a una mezcla de cianuro de sodio y el compuesto carbonílico, de modo que se genere cianuro de hidrógeno in situ. La cantidad de ácido añadida debe ser insuficiente para consumir todo el ion cianuro, por lo que se mantienen condiciones suficientemente alcalinas para una adición rápida.
También se ha demostrado que la hidrólisis catalizada por ácido de cianohidrinas sililadas (R3SiCN) es una fuente de cianuro de hidrógeno para formar cianohidrinas incluso con cetonas altamente impedidas.
2 (CH3)3SiCN + H2O → (CH3)3SiOSi(CH3)3 + 2 HCN
El cianuro de hidrógeno se añade a través del doble enlace carbono-oxígeno en aldehídos y cetonas para producir compuestos conocidos como hidroxinitrilos. Por ejemplo, con el etanal (un aldehído) se obtiene el 2-hidroxipropanenitrilo:
Con la propanona (una cetona) se obtiene el 2-hidroxi-2-metilpropanenitrilo:
La reacción no se realiza normalmente con cianuro de hidrógeno propiamente dicho, porque es un gas extremadamente venenoso. En su lugar, el aldehído o la cetona se mezclan con una solución de cianuro de sodio o de potasio en agua a la que se ha añadido un poco de ácido sulfúrico. El pH de la solución se ajusta a unos 4 – 5, ya que así se consigue la reacción más rápida. La solución contendrá cianuro de hidrógeno (de la reacción entre el cianuro de sodio o de potasio y el ácido sulfúrico), pero todavía contiene algunos iones de cianuro libres. Esto es importante para el mecanismo.
Mecanismo de formación de la cianohidrina
1) En el primer paso el ion cianuro actúa como nucleófilo y forma un enlace con el carbono carbonílico electrofílico. Los dos electrones del enlace pi del carbonilo son empujados hacia el oxígeno electronegativo formando un ion alcóxido tetraédrico intermedio.
2) El ion alcóxido es protonado por el HCN que regenera el ion cianuro.
Química adicional de las cianohidrinas
Los grupos funcionales de cianohidrina a menudo resultan útiles debido a la química adicional que puede llevarse a cabo debido a la presencia de una funcionalidad de hidroxilo y nitrilo. En particular, la deshidratación puede convertir el grupo hidroxilo en un alqueno (sección 17.6). El nitrilo puede convertirse en un grupo de función de ácido carboxílico mediante la reacción con una solución acuosa ácida caliente (sección 20.7). Además, el nitrilo puede reducirse mediante la adición de LiAlH4 para formar una amina primaria. La formación de una cianohidrina permite convertir fácilmente los aldehídos y la cetona en una gran variedad de grupos funcionales.
Otras cianohidrinas interesantes son: mandelonitrilo, cianohidrina de acetona y glicolonitrilo.
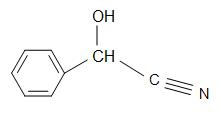

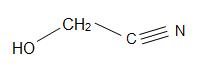
Estructuras del Madelonitrilo (izquierda), cianohidrina de acetona (centro), y glicolonitrilo (derecha)
El madelonitrilo tiene una fórmula estructural de C6H5CH(OH)CN y se encuentra en los huesos de algunas frutas. La acetona cianohidrina tiene la estructura, (CH3)2C(OH)CN, y se utiliza en la producción de metilmetacrilato (también conocido como acrílico). El glicolonitrilo es un compuesto orgánico con la fórmula estructural de HOCH2CN, que es la cianohidrina más simple que se deriva de los formaldehídos.
Problemas
Completa las siguientes reacciones para las cianohidrinas:
1)
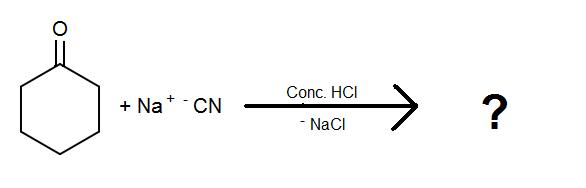
2)
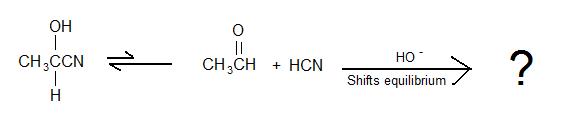
3) Verdadero o falso: Para que se forme una cianohidrina, se realiza una adición rápida de ácido fuerte a la sal de cianuro para convertir la sal en HCN.
4) Verdadero o falso: Las reacciones de cianohidrina son irreversibles.
5) ¿Cuál es el producto de la reacción global?
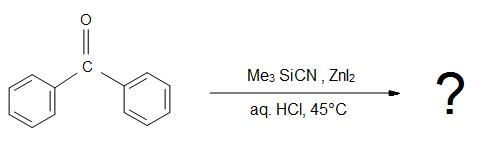
Respuestas
1)
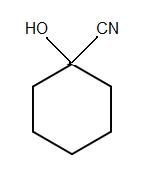
2)
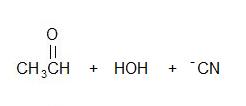
3) Falso, adición lenta
4) Falso, reversible
5)
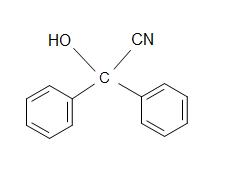
-
Dr. Dietmar Kennepohl FCIC (Profesor de Química, Universidad de Athabasca)
-
Prof. Steven Farmer (Universidad Estatal de Sonoma)
-
William Reusch, Profesor Emérito (Michigan State U.), Virtual Textbook of Organic Chemistry
-
Jim Clark (Chemguide.co.uk)