El óxido de cromo (iii), comúnmente llamado cromo y referido como oxo(oxochromiooxy)chromium en la nomenclatura IUPAC, es un compuesto inorgánico que contiene cromo y oxígeno representado por la fórmula química Cr2O3 . Se presenta de forma natural como el mineral eskolaita y es un compuesto altamente insoluble y de gran estabilidad térmica, que tiene las propiedades de un ácido y de una base .
Identificación del Cromo (III) Identificación del óxido |
|
| Número CAS | 1308-38-9 |
| PubChem CID | 517277 |
| ChemSpider ID | 451305 |
| Número ONU | 3077 |
| Número CE | 215-160-9 |
| Número RTECS | GB6475000 |
| QDOXWKRWXJOMAK-UHFFFAOYSA-N | |
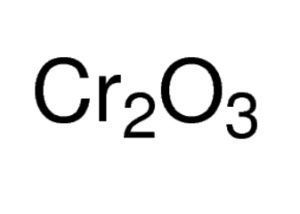
Fórmula del óxido de cromo (III)
Cómo se prepara el óxido de cromo (III)
Se produce a través de la reducción del dicromato de sodio utilizando azufre a altas temperaturas indicadas por la reacción redox :
Na2Cr2O7 + S → Na2SO4 + Cr2O3
El dicromato de amonio, al calentarse, se descompone en óxido de cromo (iii), agua y nitrógeno :
(NH4)2Cr2O7 → Cr2O3 + N2 + 4H2O
El carbonato de cromo (iii) se calienta para formar óxido de cromo (iii) y dióxido de carbono:
Cr2(CO3)3 → Cr2O3 + 3CO2
Reacción con otros compuestos
Oxido de cromo (III) con ácido clorhídrico
Reacciona con ácido clorhídrico diluido para formar cloruro de cromo (iii) y agua :
Cr2O3 + 6HCl → 2CrCl3 + 3H2O
Oxido de cromo (III) con sulfuro de hidrógeno
Cuando el óxido de cromo (iii) reacciona con sulfuro de hidrógeno gaseoso, da lugar a sulfuro de cromo (iii) y agua:
Cr2O3 + 3H2S → Cr2S3 + 3H2O
Propiedades y características del óxido de cromo (III)
Propiedades generales |
|
| Masa molecular/Peso molecular | 151.989 g/mol |
Propiedades físicas |
|
| Color y aspecto | Seco, verde claro u oscuro, polvo cristalino fino | Punto de fusión | 2,435 °C, 4.415 °F |
| Punto de ebullición | 4,000 °C, 7.230 °F |
| Densidad | 5.22 g cm-3 |
| Estado de la materia a temperatura ambiente | Sólido |
| Solubilidad | Insoluble en acetona y alcohol, muy poco soluble en álcalis y ácidos | Solubilidad en agua | Prácticamente insoluble, 2.96 µg/L (20 °C, pH 8), 3,13 µg/L (20 °C, pH 6) | Susceptibilidad magnética (χ) | 1960.0 X 10-6 cm3/mol |
Propiedades atómicas |
|
| Estructura del cristal | Hexagonal |

Oxido de cromo (III)
Usos
- Debido a su estabilidad, el óxido de cromo (iii) se utiliza como pigmento verde en tintas, vidrios y pinturas y como colorante para la cerámica, además de producir un tenue tinte verde en los esmaltes .
- Sirve como abrasivo para pulir o acariciar los bordes de maquinillas de afeitar, cuchillos y superficies de dispositivos ópticos.
Es seguro
La exposición al óxido de cromo (iii) a través de la boca y la piel puede causar toxicidad aguda . Puede causar una reacción alérgica en la piel y daños oculares graves . También puede causar toxicidad reproductiva y es perjudicial para el feto.
- Oxido de cromo (III) – Pubchem.ncbi.nlm.nih.gov
- Oxido de cromo en polvo (Cr2O3) – Reade.com/li>
- Oxido de Cromo(III) – Americanelements.com
- Química del Cromo – Chem.libretexts.org
- Oxido de Cromo(III) – Chemspider.com/li>
- Ecuaciones químicas – Chemequations.com
- Estoquiometría de la descomposición del dicromato de amonio – Dartmouth.edu
- Oxido de cromo – Chromestarchemicals.com
- 5 datos interesantes sobre el óxido de cromo verde – Basstechintl.com