Objectivos
Após completar esta secção, deverá ser capaz de
- escrever uma equação para descrever a formação de uma cianohidrina a partir de um aldeído ou cetona.
- identificar a cianidrina formada a partir da reacção de um dado aldeído ou cetona com cianeto de hidrogénio.
- identificar o aldeído ou cetona, os reagentes, ou ambos, necessários para preparar uma dada cianidrina.
- escrever o mecanismo detalhado para a adição de cianeto de hidrogénio a um aldeído ou cetona.
Termos Chave
Certifique-se de que pode definir, e utilizar no contexto, o termo chave abaixo.
- cyanohydrin
Notas de estudo
Para uma formação bem sucedida de cianidrina é importante ter iões de cianeto livres para reagir com a cetona ou aldeído. Isto pode ser conseguido usando um sal (por exemplo KCN ou NaCN) ou uma forma sililada (por exemplo Me3SiCN) de cianeto em condições ácidas ou usando HCN com alguma base adicionada para produzir o CN necessário – nucleófilo.
cianeto de hidrogénio (HC≡N), adiciona reversivelmente aos aldeídos e a muitos aductos de hidroxialcanenitrilo formadores de cetonas (vulgarmente conhecidos e chamados de cianohidrinas). As cianohidrinas têm a fórmula estrutural de R2C(OH)CN. O “R” na fórmula representa um alquil, aryl, ou hidrogénio.
Figure 19.6.1: Reacção Geral da Formação de Cianohidrina
Uma característica importante da formação de cianohidrina é que requer um catalisador básico. Uma vez que o próprio cianeto de hidrogénio é um ácido (pKa = 9,25), os melhores resultados ocorrem quando uma pequena quantidade de uma base forte activa o cianeto de hidrogénio convertendo-o em ião cianeto ((-)C≡N), que pode funcionar como um nucleófilo de carbono. Na ausência de base, a reacção não prossegue, ou é, na melhor das hipóteses, muito lenta. A formação de cianidrina é fracamente exotérmica, e é favorecida pelos aldeídos, e pelas cetonas cíclicas e metil sem obstáculos.
Em síntese prática de cianohidrinas, é conveniente adicionar um ácido forte a uma mistura de cianeto de sódio e ao composto carbonilo, de modo a que o cianeto de hidrogénio seja gerado in situ. A quantidade de ácido adicionada deve ser insuficiente para consumir todo o ião cianeto, pelo que se mantêm condições alcalinas suficientes para uma rápida adição.
Também se demonstrou que a hidrólise de cianidrinas sililadas (R3SiCN) é uma fonte de cianeto de hidrogénio para formar cianidrinas mesmo com cetonas altamente obstruídas.
2 (CH3)3SiCN + H2O → (CH3)3SiOSi(CH3)3 + 2 HCN
Cianeto de hidrogénio adiciona através da dupla ligação carbono-oxigénio em aldeídos e cetonas para produzir compostos conhecidos como hidroxinitrilos. Por exemplo, com etanal (um aldeído) obtém-se 2-hidroxipropanenitrilo:
Com propanona (uma cetona) obtém-se 2-hidroxi-2-metilpropanenitrilo:
A reacção não é normalmente feita utilizando o próprio cianeto de hidrogénio, porque este é um gás extremamente venenoso. Em vez disso, o aldeído ou cetona é misturado com uma solução de cianeto de sódio ou potássio em água à qual foi adicionado um pouco de ácido sulfúrico. O pH da solução é ajustado para cerca de 4 – 5, porque isto dá a reacção mais rápida. A solução conterá cianeto de hidrogénio (da reacção entre o cianeto de sódio ou potássio e o ácido sulfúrico), mas ainda contém alguns iões de cianeto livres. Isto é importante para o mecanismo.
Mecanismo de Formação de Cianidrina
1) No primeiro passo, o ião cianeto actua como nucleófilo e forma uma ligação com o carbono carbonilo electrofílico. Os dois electrões na ligação carbonil pi são empurrados para o oxigénio electronegativo formando um ião alcóxido tetraédrico intermédio.
2) O ião alcóxido é protonado por HCN que regenerou o ião cianeto.
Further Chemistry of Cyanohydrins
Cyanohydrin functional groups often prove useful because of the further chemistry that can be carried out due to the presence of a hydroxyl and nitrile functionality. Em particular, a desidratação pode converter o grupo hidroxil num alqueno (Secção 17.6). O nitrilo pode ser convertido num grupo de função ácido carboxílico através de reacção com uma solução aquosa ácida quente (Secção 20.7). Além disso, o nitrilo pode ser reduzido pela adição de LiAlH4 para formar uma amina primária. A formação de uma cianohidrina permite que os aldeídos e a cetona sejam facilmente convertidos numa grande variedade de grupos funcionais.
Outras cianidrinas
Outras cianidrinas interessantes são: mandelonitrilo, acetona cianidrina, e glicolonitrilo.
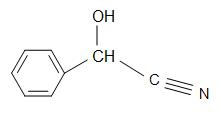

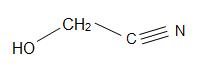
Estruturas de Madelonitrilo (esquerda), Acetona cianohidrina (centro), e glicolonitrilo (direita)
Mandelonitrilo tem uma fórmula estrutural de C6H5CH(OH)CN e ocorre em poços de algumas frutas. A cianidrina de acetona tem a estrutura, (CH3)2C(OH)CN, e é utilizada na produção de metacrilato de metilo (também conhecido como acrílico). O glicolonitrilo é um composto orgânico com a fórmula estrutural de HOCH2CN, que é a cianohidrina mais simples que é derivada pelos formaldeídos.
Problemas
Completar as seguintes reacções para as cianidrinas:
1)
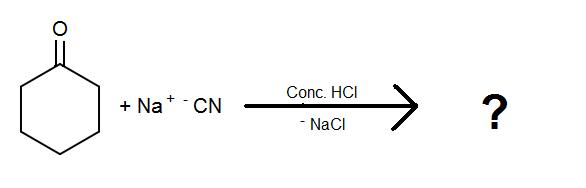
2)
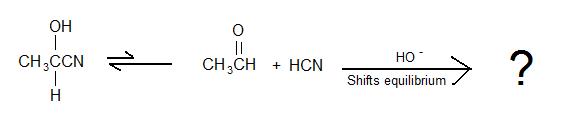
3) Verdadeiro ou Falso: Para a formação de uma cianohidrina, uma rápida adição de ácido forte ao sal de cianeto é realizada para converter o sal em HCN.
4) Verdadeiro ou Falso: As reacções de cianohidrina são irreversíveis.
5) Qual é o produto para a reacção global?
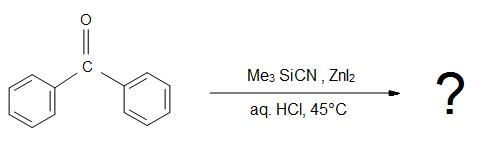
Respostas
1)
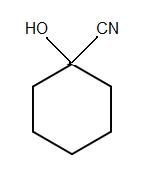
2)
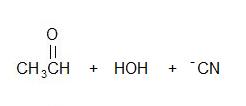
3) Falso, adição lenta
4) Falso, reversível
5)
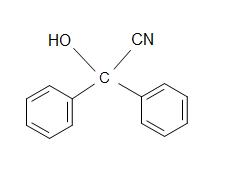
Contribuidores e Atribuições
- p>p>Dr. Dietmar Kennepohl FCIC (Professor de Química, Universidade de Athabasca)
- p>p>Prof. Steven Farmer (Sonoma State University)
- p>William Reusch, Professor Emérito (Michigan State U.), Virtual Textbook of Organic Chemistry
- p>Jim Clark (Chemguide.co.uk)