Saponificação de Gordura – Síntese de Sabão
Saponificação é o processo de fazer sabão a partir de álcali e gordura (ou óleo). Os óleos vegetais e gorduras animais são ésteres gordos sob a forma de triglicéridos. O álcali quebra a ligação éster e liberta o sal ácido gordo e o glicerol. Se necessário, os sabões podem ser precipitados através da salga com cloreto de sódio saturado. Normalmente, o hidróxido de sódio é utilizado na formação de sabão duro, enquanto o hidróxido de potássio é utilizado no caso de sabão mole.
Esquema 2. Saponification Reaction.
Mecanismo de limpeza por sabão
Não é possível remover a sujidade (especialmente óleo e gordura) utilizando apenas água. Os componentes não polares presentes na sujidade repelem o constituinte polar do solvente. Na presença de um detergente (sabão) que tem pontas polares e não polares, as pontas não polares do detergente que é repelido pela água interagem com a massa lubrificante não polar. Ao mesmo tempo, as extremidades polares são atraídas para as moléculas hidrofílicas. Assim, os dois componentes polares e não polares complementares da sujidade são dissolvidos e removidos durante a lavagem. O sabão forma micelas na água, onde as extremidades polares se alinham ao longo da circunferência e os constituintes não polares portadores das espécies não polares permanecem no centro da micela.
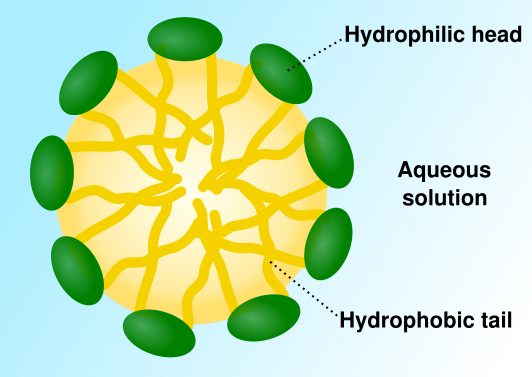
* Figura 8. Formação típica de micelas
*Fonte: http://www.images.google.com
Materiais Requeridos
-
Gordura Animal
-
Etanol
-
6N Hidróxido de sódio
-
Cloreto de sódio
-
Isoproply alcohol
-
Dois copos de 100 ml
-
Duas varetas de vidro
-
Dois frascos cónicos de 250 ml
-
Água destilada
-
Microondas
-
placa quente
-
Toalhas para limpeza
-
Parar relógio
Óculos de protecção
Procedimento experimental
Dez gramas de gordura animal disponível comercialmente foi pesada e dissolvida em 50 ml de etanol por agitação constante. A esta mistura foram adicionados 15 ml de solução de hidróxido de sódio 6N recentemente preparada. Esta mistura foi aquecida numa placa quente até que toda a gordura fosse completamente dissolvida. Foram adicionados 20 ml de água destilada e a mistura foi arrefecida num banho de gelo. A mistura arrefecida foi então vertida num copo contendo 50ml de solução de cloreto de sódio a 0,2%. O sabão foi formado após arrefecimento. A solução foi filtrada para separar o sabão do glicerol assim formado. A experiência foi repetida utilizando microondas. As correspondentes eficiências e consumos de energia foram calculados.
Resultado & Discussão
Como resultado do processo de Saponificação, os ácidos gordos são hidrolisados na presença de um álcali de modo a formar sais de álcali e álcool. Após arrefecimento da mistura dissolvida, foi observado o fim do processo de sabão sólido. A energia consumida por cada processo é tabelada abaixo.
Uma forma de testar a formação de sabão é dissolvendo o sólido em água e verificando a formação de espuma. Também pode ser confirmada através da realização do teste de pH, que envolve a dissolução do sabão numa mistura de água 1:3 e álcool isopropílico recentemente preparada. A solução de sabão dissolvido pode ser testada com o indicador de fenolftaleína e a formação do sabão é indicada pela cor da solução. Uma solução rosa escuro e límpida indica a presença de uma solução cáustica excessiva, aquela com solução incolor ou límpida amarelada indica um pH bastante neutro, a solução turva indica óleo não tratado, a solução turva e rosa indica que a reacção foi completa. Uma solução límpida, cor-de-rosa pálido indica bons resultados.
Figure 9. (a) Solução de sabão não tratada, (b) Solução cor-de-rosa perigosa com óleo não tratado, (c) Solução de sabão rosa claro
solução indicando a formação de sabão.
Tabela 4. A energia consumida para saponificação de 10g de gordura animal.
|
Dispositivo de aquecimento |
Time (min) |
Power Rating (KJ/min) |
Real Energy Consumed (KJ) |
|
Microwave Oven |
1 |
51.0 |
36 |
Hot Plate |
4 |
51.9 |
Portanto, a percentagem de energia poupada pelo forno de microondas em relação ao forno convencional, tal como é registada pelo medidor de potência,
O processo de Saponificação utilizando aquecimento convencional levou quatro vezes mais tempo a concluir do que o processo de microondas, e consumiu mais energia. A qualidade do sabão também foi testada. Da Fig. 9 (c) vemos que a solução assim formada após a adição de fenolftaleína, era uma solução rosa claro indicando a formação de bom sabão com um pH nominal na gama de 7-9. Na fig. 9 (b) vemos uma solução cor-de-rosa opaco com gotículas amarelas, indicando a presença de óleo não reagido. A solução aparece também de cor escura indicando a presença de soda cáustica excessiva. Na figura 9 (a) aparece uma solução límpida que indica a ausência de formação de sabão.
A quantidade de energia consumida pela placa de aquecimento era significativamente maior do que a consumida pelo microondas. Isto foi atribuído à interacção directa dos reagentes com a radiação de microondas.