Izomery konstytucyjne to cząsteczki, które mają ten sam wzór cząsteczkowy, ale mają inną łączność atomów w cząsteczkach. Najlepiej będzie, jeśli zilustruję ideę izomerów konstytucyjnych na przykładzie. Załóżmy, że mamy cząsteczkę o wzorze cząsteczkowym C2H6O. Zbudowanie struktur Lewisa dla tej cząsteczki ujawnia dwie możliwości połączeń atomów:
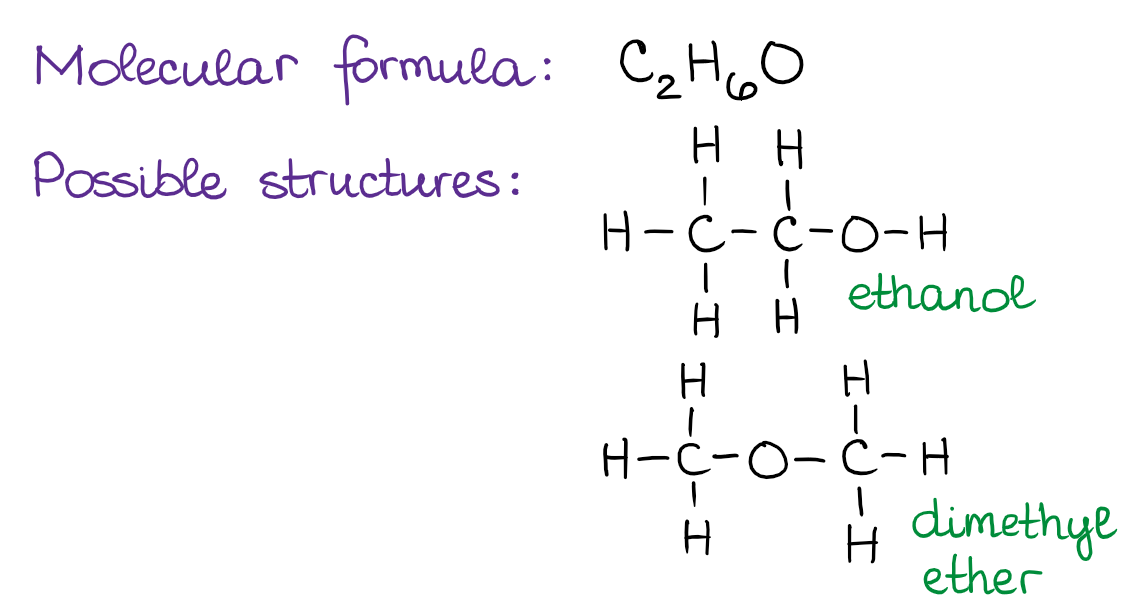
Dwie powyższe cząsteczki, etanol (alkohol etylowy) i eter dimetylowy, są przykładami izomerów konstytucyjnych. Obie mają dokładnie te same atomy w tych samych proporcjach w cząsteczce. Jednak połączenia między tymi atomami, czyli inaczej mówiąc budowa cząsteczki, jest inna. Ważną rzeczą w przypadku izomerów konstytucyjnych jest uświadomienie sobie, że są to różne cząsteczki i dlatego mają różne właściwości. Zobaczysz przykłady izomerów konstytucyjnych wiele razy w trakcie kursu, więc bardzo ważne jest, aby umieć je dostrzec.
Indeks niedoboru wodoru (HDI)lub stopień nienasycenia (DU)
Oba te terminy odnoszą się do tej samej rzeczy. Dokładny termin, którego użyje Twój instruktor, będzie zależał od jego osobistych preferencji lub wyboru książki. Podczas gdy HDI zwykle nie jest wprowadzany do czasu, gdy spojrzymy na spektroskopię, wierzę, że jest to bardzo potężne narzędzie, aby wiedzieć na początku semestru. I szczerze mówiąc, jestem trochę zdezorientowany, dlaczego to praktycznie nigdy nie jest nauczane tutaj. W każdym razie, wracając do HDI i tego, dlaczego jest takie fajne.
HDI jest użytecznym narzędziem do oszacowania motywów strukturalnych w cząsteczce. Zasadniczo, każdy stopień nienasycenia lub jednostka HDI odpowiada albo wiązaniu π, albo motywowi cyklicznemu w cząsteczce. Przypomnijmy, że wiązania podwójne i potrójne mają wiązania π. Bardziej „poprawna” definicja HDI to liczba równoważników H2 potrzebnych do nasycenia cząsteczki, aby miała ona tylko strukturę otwartych łańcuchów wiązań pojedynczych. Co, jeśli mnie pytasz, brzmi brzydko, więc nigdy więcej nie będę tego powtarzał. 🤣
Spójrzmy na kilka przykładów i zobaczmy jak cechy molekularne mają się do jednostek HDI:
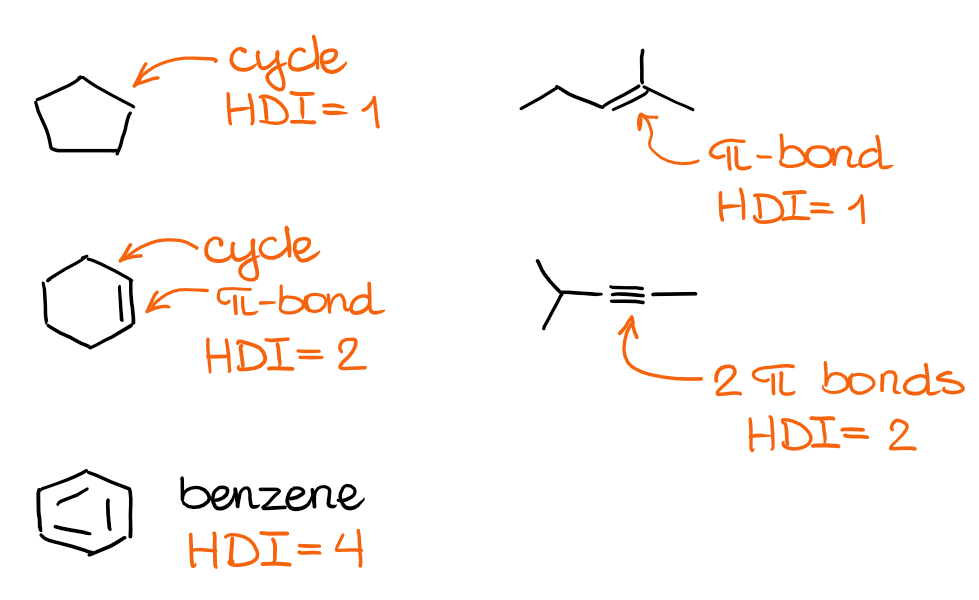
Kombinacja cykli i wiązań podwójnych lub potrójnych w twojej cząsteczce da ci wartość HDI. Ale w jaki sposób jest to przydatne dla izomerów konstytucyjnych? Cóż, ponieważ izomery konstytucyjne mają ten sam wzór molekularny, będą miały również te same indeksy HDI! W ten sposób, jeśli znamy HDI dla danej cząsteczki, możemy automatycznie narysować różne izomery konstytucyjne z odpowiednimi motywami strukturalnymi. Czy istnieje więc sposób na obliczenie HDI na podstawie samego wzoru cząsteczkowego? Z pewnością tak!
Obliczanie HDI ze wzoru cząsteczkowego
Aby obliczyć HDI używamy bardzo prostego wzoru. Warto go zapamiętać, ponieważ jest on bardzo użyteczny, szczególnie jeśli próbujesz narysować izomery konstytucyjne dla wielu różnych cząsteczek.
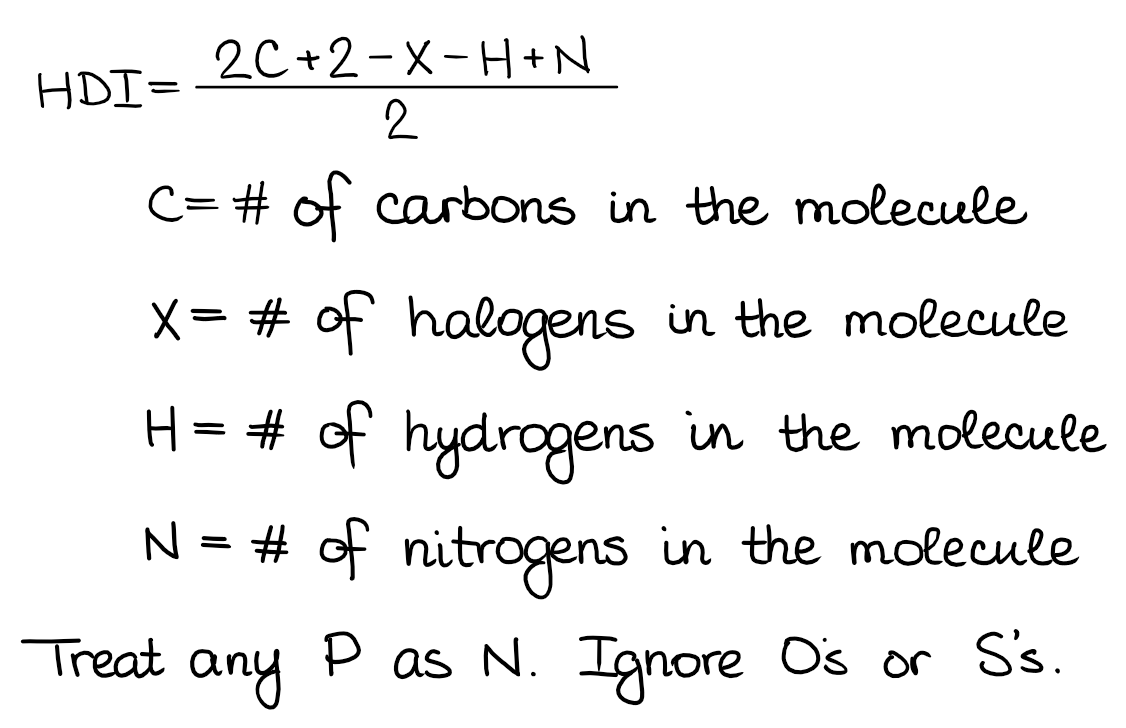
Wzór, który tu pokazuję, ma kilka różnych postaci. Więc jeśli twój instruktor lub podręcznik używa innej, nie martw się, wszystkie dają ten sam wynik. Mi osobiście podoba się ta, więc będę się jej trzymał. Przyjrzyjmy się kilku przykładom z użyciem tej formuły:
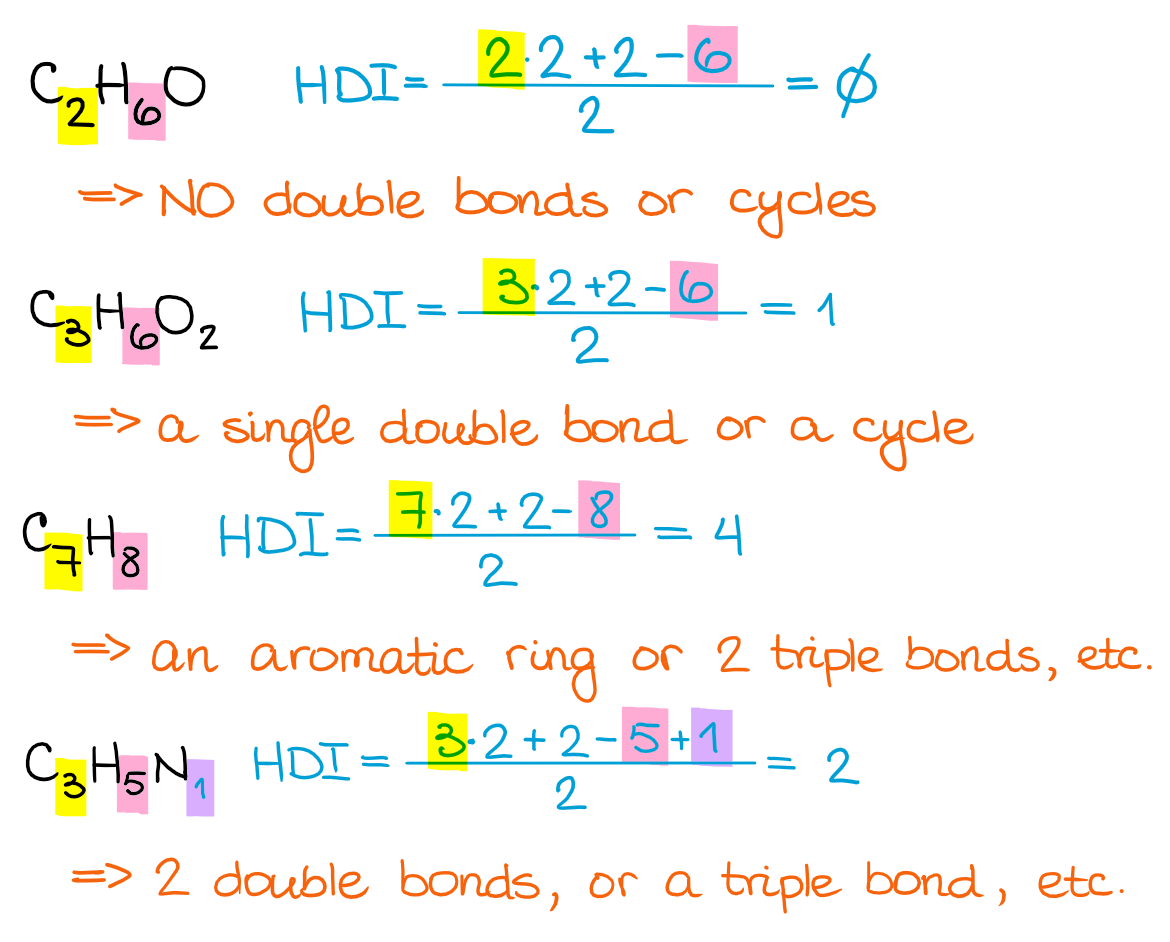
Jak widać, im wyższy HDI, tym więcej możliwości można uzyskać dla motywów strukturalnych w cząsteczce. Tak więc, chociaż jest to potężne narzędzie, nie jest to formuła „natychmiastowej odpowiedzi”, szczególnie jeśli chodzi o bardziej złożone molekuły.
Jak podejść do problemów używając formuły HDI
Więc, kiedy trzeba wymyślić możliwe izomery konstytucyjne dla molekuły, pierwszą rzeczą, na którą chcemy spojrzeć jest wzór molekularny. Stamtąd otrzymamy HDI i będziemy mieli pewne pojęcie o tym, jakich cech strukturalnych szukać w naszej cząsteczce.
Wymyślmy wszystkie możliwe izomery konstytucyjne dla cząsteczki o wzorze cząsteczkowym C3H6O.
Krok 1: Oblicz HDI ze wzoru cząsteczkowego
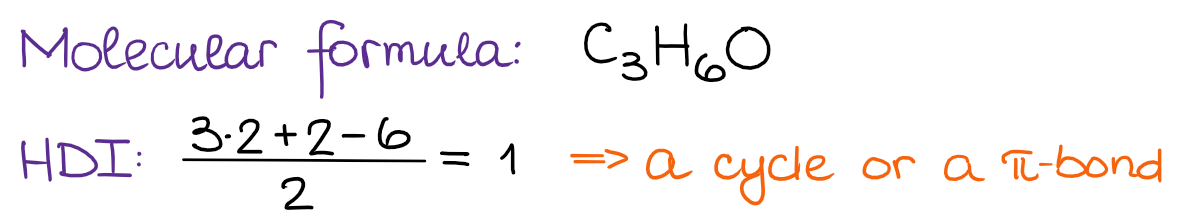
Na podstawie naszego HDI wiemy, że ta cząsteczka musi zawierać wiązanie podwójne lub cykl. Ale nie te dwa razem, ponieważ HDI = 1.
Krok 2: Narysuj możliwe izomery konstytucyjne zaczynając od liniowych (najprostszych) molekuł
Po pierwsze, zawsze wybieram możliwe struktury liniowe dla moich izomerów konstytucyjnych.
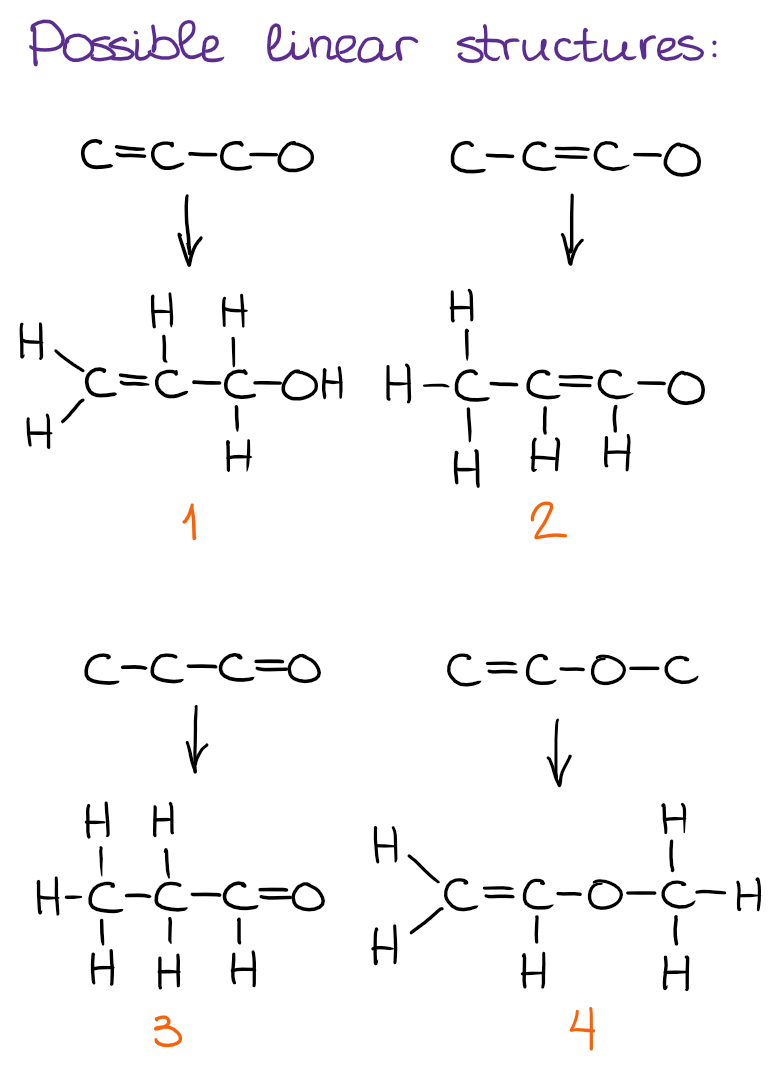
Aby to ułatwić, proponuję wymyślić rdzeń struktury, a następnie dodać niezbędną liczbę hydrogenów. Uważaj, aby nie dodać zbyt wiele i być zgodnym z wzorcami wiązań, które zwykle obserwujemy w cząsteczkach organicznych!
Jak już skończymy z liniowymi cząsteczkami, czas sprawdzić, czy możemy zrobić jakieś rozgałęzienia na boki z atomów rdzenia, które mamy w ręku:
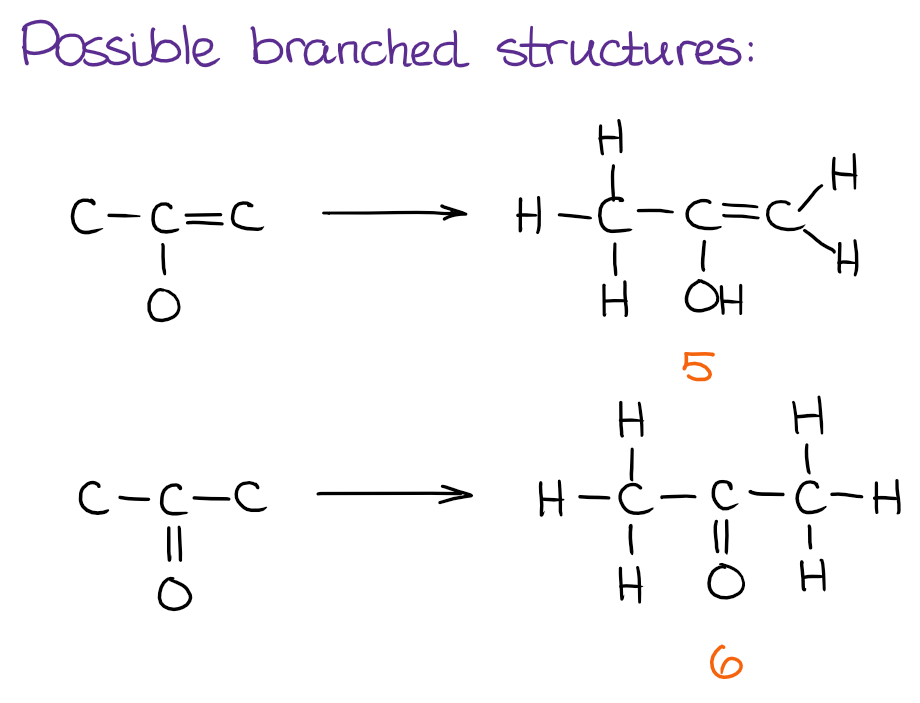
A na koniec możemy sprawdzić, czy istnieją jakieś struktury cykliczne, które możemy złożyć w całość:
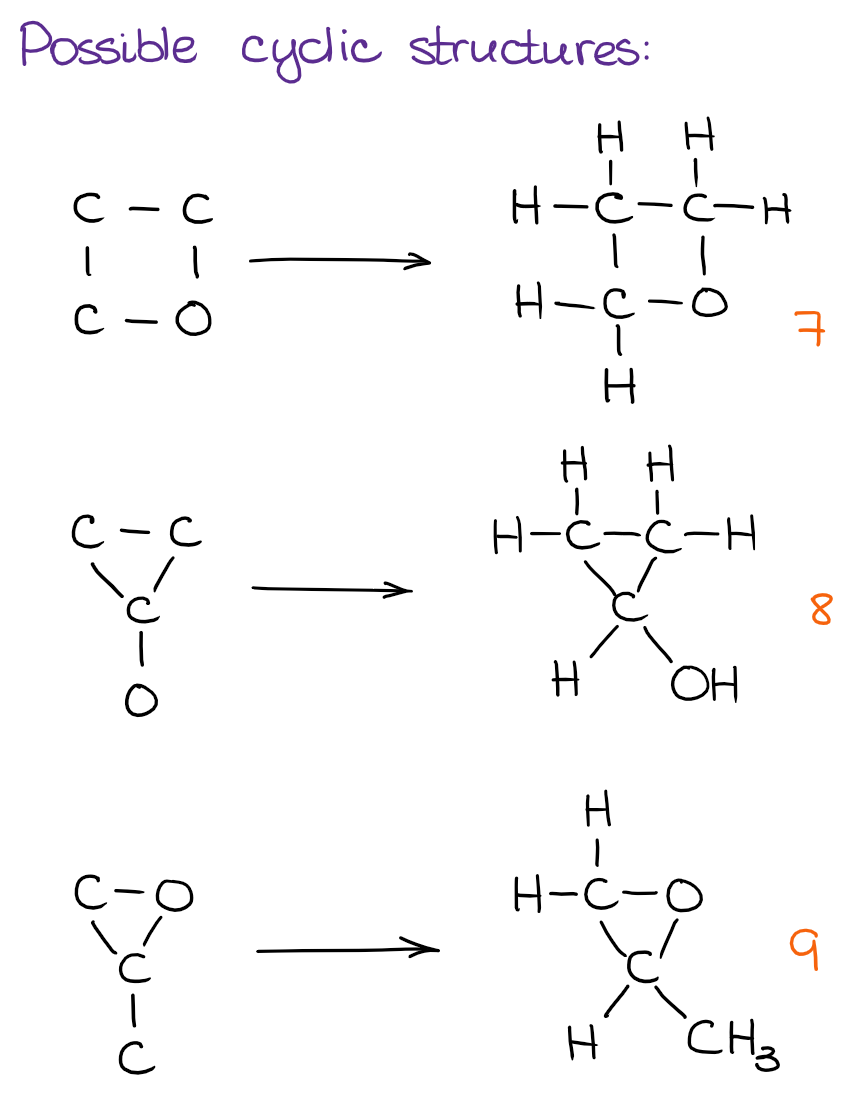
Używając tego prostego podejścia, możemy szybko i sprawnie przejść przez możliwości z bardzo małą szansą na przeoczenie jakichkolwiek struktur. Podczas gdy liczba możliwych izomerów konstytucyjnych rośnie wykładniczo wraz z liczbą atomów w cząsteczce, nie przewiduję, aby Twój instruktor dał Ci coś, co miałoby więcej niż kilkanaście struktur na teście. Jednakże, cząsteczka z 5-7 konstytucyjnymi izomerami jest dobrą grą! Jak widzisz, powyższa cząsteczka ma ich 9. I widziałem taką właśnie cząsteczkę na kilku testach w poprzednich latach. Ponadto, bądź bardzo ostrożny, jeśli twój instruktor pyta tylko o izomery konstytucyjne lub o wszystkie możliwe izomery. Jeśli nie jesteśmy ograniczeni do prostych przypadków, trzeba będzie również sprawdzić dla stereochemii, która jest nową warstwą złożoności. O tym jednak porozmawiamy innym razem.