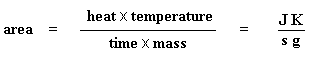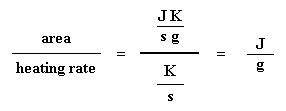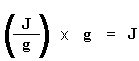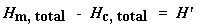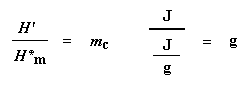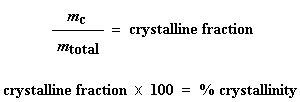Mots-clés:
amorphe,cristal,transition de premier ordre
température de transition vitreuse,capacité thermique,chaleur latente
transition de second ordre,transition thermique
Alors, comment étudier ce qui se passe dans un polymère lorsqu’on le chauffe ? La première étape serait de le chauffer, évidemment. Et c’est ce que nous faisons en calorimétrie différentielle à balayage, ou DSC pour faire court.
Nous chauffons notre polymère dans un appareil qui ressemble à quelque chose comme ceci :
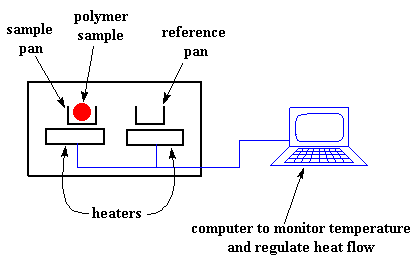
Mais surtout, il s’assure que les deux casseroles séparées, avec leurs deux chauffages séparés, chauffent à la même vitesse l’une que l’autre.
Heureusement ? Pourquoi ne chaufferaient-elles pas à la même vitesse ? La raison simple est que les deux casseroles sont différentes. L’une contient du polymère, l’autre non. L’échantillon de polymère signifie qu’il y a un matériau supplémentaire dans la coupelle. Avoir un matériau supplémentaire signifie qu’il faudra plus de chaleur pour que la température de la casserole de l’échantillon augmente au même rythme que la casserole de référence.
Donc le chauffage sous la coupelle d’échantillon doit travailler plus fort que le chauffage sous la coupelle de référence. Il doit dégager plus de chaleur. En mesurant justement la quantité de chaleur supplémentaire qu’il doit dégager, c’est ce que nous mesurons dans une expérience de DSC.
Spécifiquement, ce que nous faisons est ceci : Nous faisons un tracé au fur et à mesure que la température augmente. Sur l’axe des x, nous traçons la température. Sur l’axe des y, nous traçons la différence de production de chaleur des deux chauffages à une température donnée.
Capacité calorifique
Nous pouvons apprendre beaucoup de choses de ce tracé. Imaginons que nous chauffions un polymère.Lorsque nous commencerons à chauffer nos deux casseroles, l’ordinateur tracera la différence de puissance calorifique des deux chauffages en fonction de la température. En d’autres termes, nous traçons la chaleur absorbée par le polymère en fonction de la température. Le tracé ressemblera à quelque chose comme ceci au début.
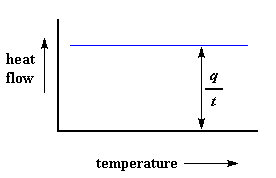
Le flux thermique à une température donnée peut nous dire quelque chose. Le flux thermique va être représenté en unités de chaleur, q fournies par unité de temps, t. Le taux de chauffage est l’augmentation de température T par unité de temps, t. Compris ?
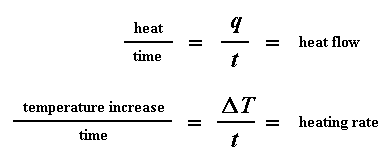
Disons maintenant que nous divisons le flux de chaleur q/t par le taux de chauffage T/t. Nous nous retrouvons avec la chaleur fournie, divisée par l’augmentation de température.
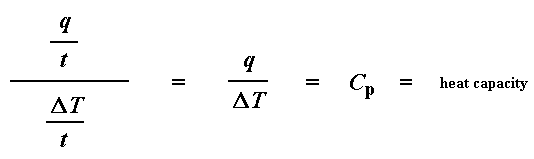
Souvenez-vous de la page sur la transition vitreuse : lorsque vous mettez une certaine quantité de chaleur dans quelque chose, sa température va augmenter d’une certaine quantité, et la quantité de chaleur nécessaire pour obtenir une certaine augmentation de température est appelée la capacité thermique, ou Cp. Nous obtenons la capacité thermique en divisant la chaleur fournie par l’augmentation de température résultante. Et c’est exactement ce que nous avons fait dans cette équation. Nous avons calculé la capacité thermique à partir du tracé DSC.
La température de transition vitreuse
Bien sûr, nous pouvons apprendre bien plus que la capacité thermique d’un polymère avec la DSC. Voyons ce qui se passe lorsque nous chauffons un peu plus le polymère. Après une certaine température, notre tracé se déplace soudainement vers le haut, comme ceci :
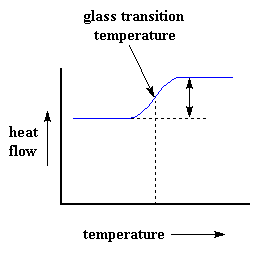
Cela signifie que nous avons maintenant plus de flux thermique. Cela signifie que nous avons également une augmentation de la capacité thermique de notre polymère. Cela arrive parce que le polymère vient de passer par la transition vitreuse. Et comme vous l’avez appris à la page sur la transition vitreuse, les polymères ont une capacité thermique plus élevée au-dessus de la température de transition vitreuse qu’en dessous. En raison de ce changement de capacité thermique qui se produit à la transition vitreuse, nous pouvons utiliser la DSC pour mesurer la température de transition vitreuse d’un polymère. Vous remarquerez que le changement n’est pas soudain, mais qu’il s’effectue sur une plage de températures. Cela rend le choix d’une Tg discrète assez délicat, mais nous prenons généralement le milieu de l’inclinaison pour être la Tg.
Cristallisation
Mais attendez il y a plus, tellement plus. Au-dessus de la transition vitreuse, lespolymères ont beaucoup de mobilité. Ils s’agitent et se tortillent, et ne restent jamais dans la même position très longtemps. Ils sont un peu comme des passagers qui essaient de s’installer confortablement dans un siège d’avion, sans jamais y parvenir, parce qu’ils peuvent bouger davantage. Lorsqu’ils atteignent la bonne température, ils auront gagné assez d’énergie pour se déplacer dans des arrangements très ordonnés, que nous appelons cristaux, bien sûr.
Lorsque les polymères entrent dans ces arrangements cristallins, ils dégagent de la chaleur. Lorsque cette chaleur est évacuée, elle rend le petit chauffage contrôlé par ordinateur sous la cuvette à échantillons très heureux. Il est heureux parce qu’il n’a pas besoin de dégager beaucoup de chaleur pour maintenir la température de la casserole en hausse. Vous pouvez voir cette chute du flux thermique comme un grand creux dans le tracé du flux thermique en fonction de la température :
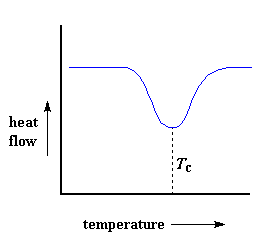
Ce creux nous dit beaucoup de choses. La température au point le plus bas du plongeon est généralement considérée comme la température de cristallisation du polymère, ou Tc. De plus, nous pouvons mesurer l’aire du creux, et cela nous indiquera l’énergie latente de cristallisation du polymère. Mais surtout, ce creux nous indique que le polymère peut effectivement cristalliser. Si vous analysiez un polymère 100 % amorphe, comme le polystyrène atactique, vous n’obtiendriez pas l’un de ces creux, car de tels matériaux ne cristallisent pas.
De plus, comme le polymère dégage de la chaleur lorsqu’il cristallise, nous appelons la cristallisation une transition exothermique.
Fusion
La chaleur peut permettre la formation de cristaux dans un polymère, mais une trop grande quantité peut les mener à leur perte. Si nous continuons à chauffer notre polymère au-delà de sa Tc, nous finirons par atteindre une autre transition thermique, celle appelée fusion. Lorsque nous atteignons la température de fusion du polymère, ou Tm, ces cristaux de polymère commencent à se désagréger, c’est-à-dire qu’ils fondent. Les chaînes sortent de leurs arrangements ordonnés et commencent à se déplacer librement. Et au cas où vous vous poseriez la question, nous pouvons repérer ce phénomène sur un tracé DSC.
Vous vous souvenez de la chaleur que le polymère dégageait lorsqu’il cristallisait ? Eh bien, lorsque nous atteignons la Tm, c’est l’heure du remboursement. Il existe une chaleur latente de fusion ainsi qu’une chaleur latente de cristallisation. Lorsque les cristaux de polymère fondent, ils doivent absorber de la chaleur pour le faire. Rappelez-vous que la fusion est une transition de premier ordre. Cela signifie que lorsque vous atteignez la température de fusion, la température du polymère n’augmente pas tant que tous les cristaux n’ont pas fondu. Cela signifie que le petit appareil de chauffage situé sous la coupelle de l’échantillon va devoir fournir beaucoup de chaleur au polymère pour faire fondre les cristaux et maintenir la température à la même vitesse que celle de la coupelle de référence. Ce flux de chaleur supplémentaire pendant la fusion se manifeste par un gros pic sur notre tracé DSC, comme ceci :
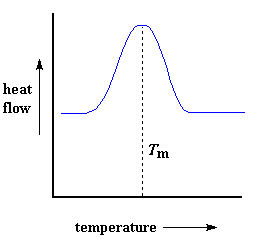
Nous pouvons mesurer la chaleur latente de fusion en mesurant l’aire de ce pic. Et bien sûr, nous prenons généralement la température au sommet du pic pour être la température de fusion du polymère, Tm.Parce que nous devons ajouter de l’énergie au polymère pour le faire fondre, nous appelons la fusion une transition endothermique.
Mettre tout ça bout à bout
Révisons donc maintenant : nous avons vu une étape dans le graphe lorsque le polymère a été chauffé au-delà de sa température de transition vitreuse. Puis nous avons vu un grand creux lorsque le polymère a atteint sa température de cristallisation. Et enfin, nous avons vu un pic important lorsque le polymère a atteint sa température de fusion. Pour les mettre ensemble, un tracé complet ressemblera souvent à quelque chose comme ceci :
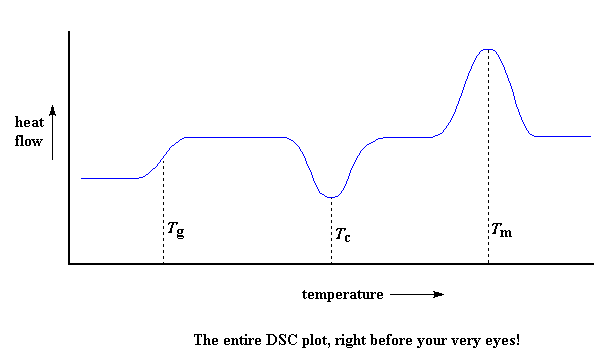
Bien sûr, tout ce que vous voyez ici ne figurera pas sur tous les tracés DSC. Le creux de cristallisation et le pic de fusion n’apparaîtront que pour les polymères qui peuvent former des cristaux. Les polymères complètement amorphes ne montreront aucune cristallisation, ni aucune fusion non plus. Mais lespolymères avec des domaines à la fois cristallins et amorphes, montreront toutes les caractéristiques que vous voyez ci-dessus.
Si vous regardez le tracé DSC, vous pouvez voir une grande différence entre la transition vitreuse et les deux autres transitions thermiques, la cristallisation et la fusion. Pour la transition vitreuse, il n’y a pas de creux, et il n’y a pas de pic non plus. Cela est dû au fait qu’il n’y a pas de chaleur latente dégagée ou absorbée par le polymère pendant la transition vitreuse. La fusion et la cristallisation impliquent toutes deux de dégager ou d’absorber de la chaleur.La seule chose que nous observons à la température de transition vitreuse est un changement de la capacité thermique du polymère.
Parce qu’il y a un changement de capacité thermique, mais qu’il n’y a pas de chaleur latente impliquée dans la transition vitreuse, nous appelons la transition vitreuse une transition de second ordre. Les transitions comme la fusion et la cristallisation, qui ont des chaleurs latentes, sont appelées des transitions de premier ordre.
Quel est le degré de cristallinité ?
La DSC peut également nous dire quelle proportion d’un polymère est cristalline et quelle proportion est amorphe. Si vous avez lu la page traitant de la cristallinité des polymères, vous savez que de nombreux polymères contiennent à la fois des matériaux amorphes et cristallins. Mais quelle est la proportion de chacun ? La DSC peut nous le dire. Si nous connaissons la chaleur latente de fusion, ΔHm, nous pouvons trouver la réponse.
La première chose que nous devons faire est de mesurer l’aire de ce grand pic que nous avonspour la fusion du polymère. Maintenant, notre graphique est un graphique du flux de chaleur par gramme de matériau, en fonction de la température. Le flux thermique est la chaleur dégagée par seconde, donc l’aire du pic est donnée en unités de chaleur x température x temps-1 x masse-1. Nous mettons généralement cela en unités telles que joules x kelvins x (secondes)-1 x (grammes)-1:
Vous avez compris ? Ne vous inquiétez pas. C’est plus simple. Nous divisons habituellement la surface par la vitesse de chauffage de notre expérience de DC. Le taux de chauffage est en unités de K/s. L’expression devient donc plus simple: Nous avons maintenant un nombre de joules par gramme. Mais comme nous connaissons la masse de l’échantillon, nous pouvons faire plus simple. Nous multiplions simplement ce chiffre par la masse de l’échantillon : Nous venons de calculer la chaleur totale dégagée lors de la fusion du polymère.Neat, huh ? Maintenant, si nous faisons le même calcul pour notre bain que nous avons obtenu sur le tracé DSC pour la cristallisation du polymère, nous pouvons obtenir la chaleur totale absorbée pendant la cristallisation. Nous appellerons la chaleur totale dégagée pendant la fusion Hm, total, et nous appellerons la chaleur de la cristallisation Hc, total. Pourquoi vient-on de faire ça ? Et que signifie ce nombre H’ ? H’ est la chaleur dégagée par la partie de l’échantillon de polymère qui était déjà à l’état cristallin avant que nous ne chauffions le polymère au-dessus de la Tc. Nous voulons savoir quelle proportion du polymère était cristalline avant d’en induire une plus grande quantité. C’est pourquoi nous soustrayons la chaleur dégagée lors de la cristallisation. Est-ce que tout le monde me suit ? Maintenant avec notre nombre magique H’ on peut calculer le pourcentage de cristallinité. On va le diviser par la chaleur spécifique de fusion, Hc*.La chaleur spécifique de fusion ? C’est la quantité de chaleur dégagée par une certaine quantité, généralement un gramme, d’un polymère. H’ est en joules, et la chaleur spécifique de fusion est généralement donnée en joules par gramme, nous allons donc obtenir une réponse en grammes, que nous appelleronsmc.
C’est la quantité totale de grammes de polymère qui étaient cristallins sous la Tc. Maintenant, si nous divisons ce nombre par le poids de notre échantillon, mtotal, nous obtenons la fraction de l’échantillon qui était cristalline, puis bien sûr, le pourcentage de cristallinité : Et c’est ainsi que nous utilisons la DSC pour obtenir le pourcentage de cristallinité.
Retour au répertoire du niveau cinq
Retour au répertoire Macrogalleria