La dissociation est la décomposition d’un composé en éléments
Le mot dissocier et dissocier ont une signification similaire – retirer d’être connecté.
Lorsqu’un composé se dissocie, les liaisons sont rompues.
Dissociation des composés ioniques
Tous les composés ioniques se dissocient dans une certaine mesure lorsqu’ils se dissolvent dans l’eau.
Les composés ioniques sont les composés qui sont constitués d’atomes appelés ions avec des charges opposées.
Lorsqu’un composé ionique se dissocie dans l’eau, la liaison ionique est rompue.
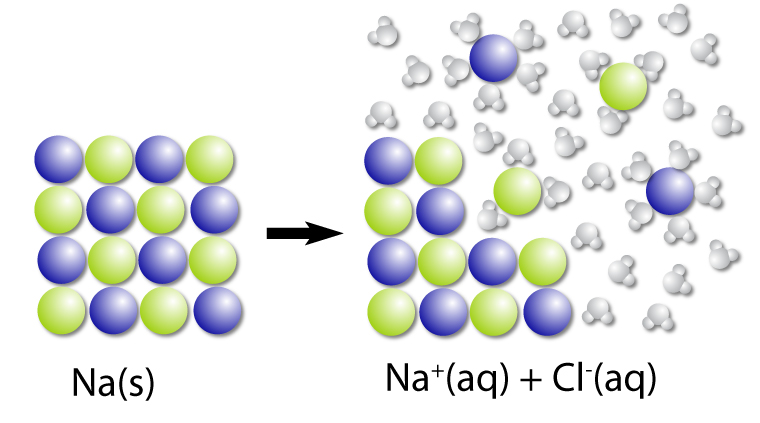
Dissociation du NaCl

Le chlorure de sodium solide se dissout dans l’eau pour produire des ions Na+ et Cl-.
La dissociation du NaCl peut s’écrire comme suit :
NaCl(s) → Na+(aq) et Cl-(aq)
- (s) représente l’état solide
- (aq) représente une solution aqueuse
- Une solution aqueuse est une solution dont le solvant est l’eau
Dissociation des composés covalents
Généralement, les composés covalents ne se dissocient pas lorsqu’ils sont dissous dans l’eau. Ceci est vrai dans la plupart des cas. Cependant il existe certains composés covalents (comme les acides chlorhydriques) qui se dissocient lorsqu’ils sont dissous dans l’eau.
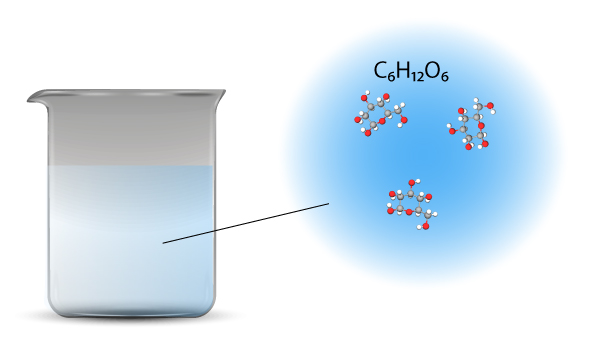
Le glucose est un composé covalent. Lorsqu’il est dissous dans l’eau, il ne se dissocie pas. Les molécules sont séparées dans l’eau – elles s’éloignent les unes des autres mais aucune liaison n’est rompue. Chaque molécule de glucose reste comme une unité entière dans l’eau.
For more reading, please refer to sodium chloride dissociation in the process of solvation.
.